组织扩张术改善穿支皮瓣供区
引言
每个人身上平均可发现390个主要穿支血管,皮瓣供区可选择穿支体区[1]或特定穿支血管供血的皮肤区域[2]。这意味着只要有必要的穿支血管存在,目前穿支皮瓣的供区选择可以最好地匹配受区的特征,例如颜色、体积、耐用性、质地等;由于穿支皮瓣供区的选择相对容易,选择过程的进一步改进聚焦于最大限度地减少供区的残留畸形。不仅必须保留供区的功能,而且由此产生的畸形应尽可能不引人注意。因为穿支皮瓣不携带肌肉,所以始终保留了供区的最大功能。供区的目标应该是获得尽可能短的线性瘢痕。
穿支皮瓣供区的简单一期闭合并不总是可以实现,尤其是当皮瓣太大而不允许这样做时。皮肤移植一直是解决方案;但该方案不但非美学,而且可能导致日后出现瘢痕挛缩、植皮区与深层肌肉粘连并限制运动[3],儿童生长迟缓[4,5],或筋膜下剥离后植皮下方肌肉膨胀导致轮廓畸形等问题[6]。为了避免皮肤移植而尝试在过度张力下一期闭合供区,这将会导致灾难性的筋膜室综合征[7]。尽管皮瓣在浅筋膜层完成了切取,单独的阔筋膜叠瓦状缝合仍然可以充分缩小供区,以允许两侧皮肤靠近[8]。近几年,附连到伤口边缘的自动或自紧的持续外部组织扩张器可以介导皮肤拉伸效应,随着时间的推移逐渐允许供区直接闭合(DermaClose®,Synovis/Micro Companies Alliance,伯明翰,阿拉巴马州,美国)[9],该设备尽管可以使用,但也很昂贵。供区附近组织瓣的同步移位也可以避免皮肤移植[10-13],但需要额外切取皮瓣的过程,并由此产生更长的瘢痕。窄的分叶穿支皮瓣可以并排放置,以增加所需的全部皮瓣覆盖面积,同时允许直接关闭供区[14-16],尽管可能性较小,因为必须存在多个紧密排列的主要穿支血管。
减少畸形的另一个考虑因素是组织扩张,特别是在供区附近没有其他主要穿支的情况下。组织扩张,例如怀孕的后遗症,是一个古老的(无意双关语)和众所周知的现象。增加的皮肤表面积,究竟是由净组织增益创造而来还是仅仅是急性负荷循环的结果,仍然存在争议[17,18]。几十年来,这种能力已成功用于游离皮瓣供区,包括穿支皮瓣[19-22],最近也用于带蒂穿支皮瓣供区[23,24]。
方法
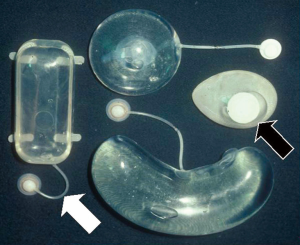
要开始组织扩张,首先必须将扩张器放置在选择扩张的皮肤下。这可以遵循以下3种模式,即皮瓣转移前、皮瓣转移时或皮瓣转移后,根据穿支皮瓣切取的时间略有不同[25]。典型的扩张器球囊有一个硅胶外壳,带有一个内部或外部的单向阀,可以将生理盐水注入其中以给球囊充气(图1)。外部阀通过长管连接到球囊,因此它可以放置在远离植入物品袋的地方,以避免注射针不小心刺穿外壳的风险,在实现显著扩张时,这是特别需要注意的问题。可用一种使用内在压缩二氧化碳气体而不是以盐水作为介质的新型无针扩张器,但目前仅用于乳房重建[26]。虽然传统的扩张器有各种形状和尺寸(图1),但矩形设计是最有用的。所需的尺寸通常取决于要扩张的皮肤的位置和皮肤的可用度。建议尽可能使用大的矩形扩张器,必要时甚至建议使用多个;但如果使用较小的扩张器也可行,则优先考虑,因为在球囊破裂之前,每个人都可以扩张到超出规定容量的许多倍(图2)[27]。
转移前扩张
潜在穿支皮瓣的设计是标记在使用常规方法证实的特定穿支周围。扩张器口袋放置的位置不得靠近穿支;不仅是为了确保在创建口袋时穿支不受损伤,而且因为可预料到的由扩张本身引起的炎症反应和瘢痕,可能为后期解剖穿支带来不必要的困难[21]。扩张器囊本身将会作为一个模板来确定所涉及的皮下区域,该区域能更好地接受它而不会起皱。扩张器囊的放置切口远离并垂直于设计皮瓣的边缘,这样将会更好地允许其形成所需扩张尺寸,最简单的是在直接可视化下,同时将外部阀放置在扩张器囊下方并且距离足够远,防止球囊被意外刺破,同时仍然很容易触及,方便以后轻松插入针头。
转移时扩张
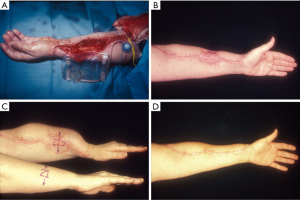
在皮瓣切取的同时,皮下组织下方的筋膜口袋从皮瓣切取后遗留的开放伤口边缘处开始制备(图3)。筋膜口袋应该稍微超出扩张器的尺寸,以再次确保扩张器的边缘既不会起皱,也不会靠近必须进行植皮的供区。外部阀也必须放置在远离扩张器囊和创面边界的位置。首先缝合皮下组织与深筋膜层,然后使用水平半埋褥式缝合真皮层与浅筋膜层,至少两层缝合是必须的。必须埋藏皮下组织的痕迹,以确保如果一层裂开,也不会无意中暴露植入物,供区皮肤移植愈合处可用来密封扩张器囊的放置部位。
转移后扩张
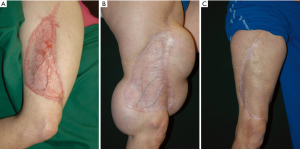
对于通常采用植皮术闭合供区且已愈合的穿支皮瓣,可以在其周围关键位置放置所需数量的扩张器(图4)。该方法与移植前扩张的方法相同,只是切口不应位于或靠近皮肤移植区与正常皮肤的交界处。一旦扩张开始,该部位通常会愈合不良或容易裂开,导致植入物暴露。
手术方法
在开始扩张之前采取保守的做法是合理的。通常是在放置扩张器囊后的2周内,但不要在所有切口或皮肤移植连接处似乎都没有完全愈合之前。如果选择增加生理盐水注射剂量,确定要注入的安全填充剂量的最佳时机是当患者感觉到不舒服时[28]。扩张器上方的皮肤缺乏毛细血管回流也应该是一个考虑因素,尤其是在忍耐力强的患者中。精细的监测方法,如经皮组织氧测量是准确的,但并不如疼痛发作时敏感[28]。注入的频率也取决于所使用的设备,但应至少定期监测患者的不良事件。
扩张的终点可能具有欺骗性。对于四肢,扩张侧肢体周长的测量值必须略大于同一水平对侧肢体周长与植皮缺损的宽度的总和(图3)。对于非四肢皮肤缺损,尽可能估计得到扩张器覆盖的距离。在这两种情况下,更多地扩张皮肤的任何潜在方法都是可取的。
切取穿支皮瓣或去除畸形皮肤移植物时,利用术后形成的伤口边缘取出植入物和注射阀。在此步骤之前,将生理盐水最大限度地注入阀门可能会获得1 cm左右的急性皮肤拉伸。然后供区实现无张力的皮肤闭合;但如果遇到这种情况,最明智的做法是留下一些皮肤移植物,稍后再回来进行连续切除。
讨论
有许多不同的方法可以实现组织扩张,组织扩张也有许多不同的设备和技术手段。使用你所熟悉的方法。例如,扩张器可以放置在肌肉下方,这能自动确保肌皮穿支不受损伤。同样,它们也可以放置在筋膜下,这是一个易于解剖且相对出血少的平面。然而,在这两种情况下,拉伸和随后的扩张受限可能会更困难和痛苦。
扩张期间的并发症是可以预料的,并且能够很好避免。正如之前强调的那样,植入物周围伤口裂开、注射阀门裸露或挤压必须及时妥善处理,否则感染不可避免。注射阀门和扩张囊都可能泄漏,导致放气,通常与针头注射相关[29]。过度扩张会导致皮肤缺血和坏死。扩张完成后的并发症包括急进地尝试伤口闭合,这不太可能导致筋膜室综合征,但更可能导致伤口边缘皮肤坏死、裂开与迁延不愈。
选择组织扩张至少需要2次不太方便的外科手术,即扩张器植入和扩张器取出。频繁的门诊和临床随访是必须的,随访频率取决于扩张器装置。这通常是一个漫长的过程,要持续数月,直到认为扩张足够[25]。患者和外科医生都必须有耐心和依从性。这对于那些正在接受转移前或转移后扩张的患者来说会更容易,这基本上会是一个选择性的、充分知情同意的决定,若没有足够时间发展有意义、和谐的医患关系,转移时扩张模式是不可能实现的。必须认识到,组织扩张不是解决所有穿支皮瓣供区闭合难题的灵丹妙药,而是众多经过长年累月试验的方案中的一种,必须予以考虑。
Acknowledgments
Thanks to David C. Rice, B.S., P.E., Sacred Heart Hospital, Allentown, Pennsylvania, who assisted with the microsurgical aspects.
Funding: None.
Footnote
Provenance and Peer Review: This article was commissioned by the editorial office, Journal of Xiangya Medicine for the series “Perforator Flap”. The article has undergone external peer review.
Conflicts of Interest: The author has completed the ICMJE uniform disclosure form (available at http://dx.doi.org/10.21037/jxym.2018.03.02). The series “Perforator Flap” was commissioned by the editorial office without any funding or sponsorship. GH served as an unpaid Guest Editor of the series and serves as an unpaid editorial board member of Journal of Xiangya Medicine from Apr 2017 to Mar 2019. The author has no other conflicts of interest to declare.
Ethical Statement: The author is accountable for all aspects of the work in ensuring that questions related to the accuracy or integrity of any part of the work are appropriately investigated and resolved.
Open Access Statement: This is an Open Access article distributed in accordance with the Creative Commons Attribution-NonCommercial-NoDerivs 4.0 International License (CC BY-NC-ND 4.0), which permits the non-commercial replication and distribution of the article with the strict proviso that no changes or edits are made and the original work is properly cited (including links to both the formal publication through the relevant DOI and the license). See: https://creativecommons.org/licenses/by-nc-nd/4.0/.
References
- Saint-Cyr M, Wong C, Schaverien M, et al. The perforasome theory: vascular anatomy and clinical implications. Plast Reconstr Surg 2009;124:1529-44. [Crossref] [PubMed]
- Taylor GI, Palmer JH. The vascular territories (angiosomes) of the body: experimental study and clinical applications. Br J Plast Surg 1987;40:113-41. [Crossref] [PubMed]
- Kimata Y, Uchiyama K, Ebihara S, et al. Anterolateral thigh flap donor-site complications and morbidity. Plast Reconstr Surg 2000;106:584-9. [Crossref] [PubMed]
- Zhao Y, Qiao Q, Liu Z, et al. Alternative method to improve the repair of the donor site of the anterolateral thigh flap. Ann Plast Surg 2002;49:593-8. [Crossref] [PubMed]
- Novak CB, Lipa JE, Noria S, et al. Comparison of anterolateral thigh and radial forearm free flap donor site morbidity. Microsurgery 2007;27:651-4. [Crossref] [PubMed]
- Lipa JE, Novak CB, Binhammer PA. Patient-reported donor-site morbidity following anterolateral thigh free flaps. J Reconstr Microsurg 2005;21:365-70. [Crossref] [PubMed]
- Addison PD, Lannon D, Neligan PC. Compartment syndrome after closure of the anterolateral thigh flap donor site: a report of two cases. Ann Plast Surg 2008;60:635-8. [Crossref] [PubMed]
- Rodriguez ED, Bluebond-Langner R, Park J, et al. Does fascia lata repair facilitate closure and does it affect compartment pressures of the anterolateral thigh flap donor site? Plast Reconstr Surg 2007;120:1300-4. [Crossref] [PubMed]
- Senchenkov A, Agag RL, Lee J, et al. Management of anterolateral thigh free flap donor site defects with a continuous external tissue expander. Microsurgery 2015;35:290-4. [Crossref] [PubMed]
- Yamada N, Kakibuchi M, Kitayoshi H, et al. A new way of elevating the anterolateral thigh flap. Plast Reconstr Surg 2001;108:1677-82. [Crossref] [PubMed]
- Hanasono MM, Skoracki RJ, Yu P. A prospective study of donor-site morbidity after anterolateral thigh fasciocutaneous and myocutaneous free flap harvest in 220 patients. Plast Reconstr Surg 2010;125:209-14. [Crossref] [PubMed]
- Calderón W, Borel C, Roco H, et al. Primary closure of donor site in anterolateral cutaneous thigh free flap. Plast Reconstr Surg 2006;117:2528-9. [Crossref] [PubMed]
- Hallock GG. Closure of the ulnar forearm free flap donor site using a local radial forearm flap. Br J Plast Surg 1992;45:94-6. [Crossref] [PubMed]
- Marsh DJ, Chana JS. Reconstruction of very large defects: a novel application of the double skin paddle anterolateral thigh flap design provides for primary donor-site closure. J Plast Reconstr Aesthet Surg 2010;63:120-5. [Crossref] [PubMed]
- Sano K, Hallock GG, Hamazaki M, et al. The perforator-based conjoint (chimeric) medial Sural(MEDIAL GASTROCNEMIUS) free flap. Ann Plast Surg 2004;53:588-92. [Crossref] [PubMed]
- Zhang YX, Hayakawa TJ, Levin LS, et al. The Economy in Autologous Tissue Transfer: Part 1. The Kiss Flap Technique. Plast Reconstr Surg 2016;137:1018-30. [Crossref] [PubMed]
- Austad ED, Thomas SB, Pasyk K. Tissue expansion: dividend or loan? Plast Reconstr Surg 1986;78:63-7. [Crossref] [PubMed]
- Hirshowitz B, Kaufman T, Ullman J. Reconstruction of the tip of the nose and ala by load cycling of the nasal skin and harnessing of extra skin. Plast Reconstr Surg 1986;77:316-21. [Crossref] [PubMed]
- Hallock GG. Free flap donor site refinement using tissue expansion. Ann Plast Surg 1988;20:566-72. [Crossref] [PubMed]
- Leighton WD, Russell RC, Feller AM, et al. Experimental pretransfer expansion of free-flap donor sites: II. Physiology, histology, and clinical correlation. Plast Reconstr Surg 1988;82:76-87. [Crossref] [PubMed]
- Hallock GG. The preexpanded anterolateral thigh free flap. Ann Plast Surg 2004;53:170-3. [Crossref] [PubMed]
- Hallock GG. Refinement of the radial forearm flap donor site using skin expansion. Plast Reconstr Surg 1988;81:21-5. [Crossref] [PubMed]
- Kulahci Y, Sever C, Uygur F, et al. Pre-expanded pedicled thoracodorsal artery perforator flap for postburn axillary contracture reconstruction. Microsurgery 2011;31:26-31. [Crossref] [PubMed]
- Sever C, Kulahci Y, Eren F, et al. Reconstruction of postburn cervical contractures using expanded supraclavicular artery flap. J Burn Care Res 2013;34:e221-7. [Crossref] [PubMed]
- Hallock GG. Tissue expansion techniques to minimize morbidity of the anterolateral thigh perforator flap donor site. J Reconstr Microsurg 2013;29:565-70. [Crossref] [PubMed]
- Ascherman JA, Zeidler K, Morrison KA, et al. Carbon Dioxide-Based versus Saline Tissue Expansion for Breast Reconstruction: Results of the XPAND Prospective, Randomized Clinical Trial. Plast Reconstr Surg 2016;138:1161-70. [Crossref] [PubMed]
- Hallock GG. Maximum overinflation of tissue expanders. Plast Reconstr Surg 1987;80:567-9. [Crossref] [PubMed]
- Hallock GG, Rice DC. Objective monitoring for safe tissue expansion. Plast Reconstr Surg 1986;77:416-20. [Crossref] [PubMed]
- Hallock GG. Puncture threshold prior to leakage from tissue expander reservoirs. Plast Reconstr Surg 1988;82:666-8. [Crossref] [PubMed]
贺继强
硕士及博士均就读于中南大学湘雅医院手显微外科。博士就读期间,在国家留学基金委的资助下赴美国约翰霍普金斯大学整形外科学习2年4个月。约翰霍普金斯大学整形外科是世界知名的同种异体手移植中心,我所在的同种异体复合组织移植实验室聚焦于显微外科培训,复合组织移植的基础与临床,器官与组织的低温保存和机器灌注。在美国学习期间整理湘雅医院手显微外科的解剖学和临床病例资料,发表sci论文数篇。(更新时间:2021/9/6)
(本译文仅供学术交流,实际内容请以英文原文为准。)
Cite this article as: Hallock GG. Tissue expansion for improvement of the perforator flap donor site. J Xiangya Med 2018;3:11.